20 de agosto de 2025
Un hallazgo revela cómo el músculo puede transformarse en hueso y acelerar la reparación de fracturas graves
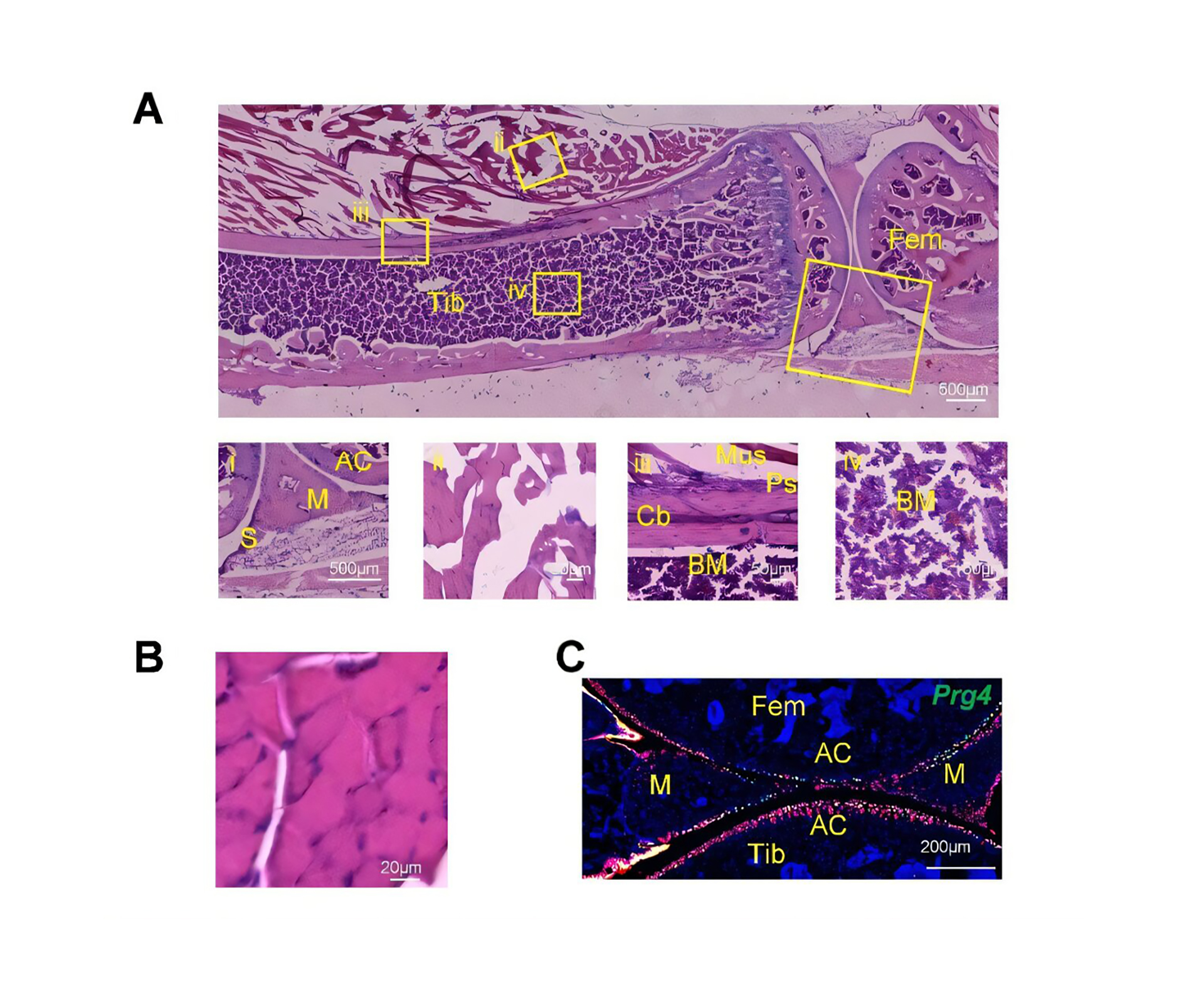
Un grupo de científicos de la Universidad de Pensilvania identificó cómo ciertas células madre presentes en el músculo pueden contribuir a la reparación ósea en lesiones que hasta ahora presentaban dificultades para su recuperación
La investigación, publicada en De acuerdo con el equipo dirigido por Ling Qin, profesora titular del Departamento de CirugÃa Ortopédica, las células Prg4+ representan un subtipo de fibro-adipogenic progenitor (FAP). Estas células madre residen normalmente en los músculos que rodean el esqueleto y, en situaciones de daño, migran rápidamente hacia el lugar de la fractura. Una vez allÃ, se transforman en los diferentes tipos de células necesarias para regenerar el hueso: condrocitos, osteoblastos y osteocitos.
El trabajo detalla que “las células podÃan realmente transformarse de células musculares a células óseasâ€, una observación que desafÃa la idea tradicional de que la mayor parte de la reparación de fracturas recae en las células madre del periostio, la capa que recubre los huesos.En palabras del artÃculo original: “Prg4+ respondÃa rápidamente a las lesiones esqueléticas, migrando primero al sitio de fractura desde el músculo esqueléticoâ€. Allà formaban los diferentes tipos de células que generan el callo óseo temporal, la estructura que facilita la unión entre los extremos rotos durante la curación.
Una vez que el hueso habÃa logrado regenerarse completamente, los investigadores observaron que las células originalmente provenientes de Prg4+ ya convertidas en óseas permanecÃan en la zona, listas para participar si ocurrÃa otra fractura. El informe señala: “Se observó en huesos curados que las células provenientes de Prg4+ producÃan osteoblastos y osteocitos, quedando listas para reparar posibles fracturas futurasâ€.Para verificar la importancia de las Prg4+ en la curación, el equipo de Qin realizó un experimento clave. Al eliminar deliberadamente estas células en los ratones que sufrÃan fracturas, la curación se hizo lenta y menos eficiente. El estudio informa: “Al destruir a propósito las células Prg4+, se ralentizó de manera significativa la actividad de reparación y cicatrizaciónâ€. Este efecto permitió comprobar la función esencial de estas células en situaciones donde la restauración del hueso resulta especialmente difÃcil.Mirando al futuro, las investigaciones proyectan el desarrollo de terapias que puedan estimular las células Prg4+ desde el propio organismo con la ayuda de medicamentos especÃficos, denominados factores de crecimiento, o bien la posibilidad de introducir células ya activadas directamente en la zona de la fractura para favorecer la formación de nuevo hueso.
El equipo interdisciplinario planea explorar ahora las capacidades de reparación de otros tipos de fibro-adipogenic progenitor para ampliar las opciones en el tratamiento de lesiones óseas, según destacaron.




